Ведущий эксперт в области детской офтальмологии и генной терапии, доктор медицинских наук Доминик Бремон-Жиньяк, рассказывает о том, как инновационные методы генной терапии — например, Лукстурна при дистрофии сетчатки и Аталурен при аниридии — меняют подход к лечению редких заболеваний глаз. Эти методы дают надежду на восстановление зрения у детей в тех случаях, когда традиционная терапия оказывается бессильной.
Генная терапия заболеваний глаз: современные подходы и перспективы
Перейти к разделу
- Обзор генной терапии в офтальмологии
- Лукстурна при дистрофии сетчатки, вызванной мутацией RPE65
- Результаты клинических испытаний и исходы лечения пациентов
- Аталурен и генная терапия аниридии
- Будущее генной терапии заболеваний глаз
- Новая надежда для пациентов с редкими заболеваниями глаз
- Полная расшифровка
Обзор генной терапии в офтальмологии
Генная терапия — это революционный прорыв в лечении редких заболеваний глаз, причём глаз служит идеальной миниатюрной лабораторией для медицинских исследований. Доктор медицинских наук Доминик Бремон-Жиньяк подчёркивает значительный прогресс в этой области, отмечая, что первое фармацевтическое средство для офтальмологической генной терапии было одобрено совсем недавно. Этот шаг знаменует важнейшую веху в офтальмологии — переход от теоретических изысканий к практическому, меняющему жизнь лечению пациентов с генетическими нарушениями зрения.
Лукстурна при дистрофии сетчатки, вызванной мутацией RPE65
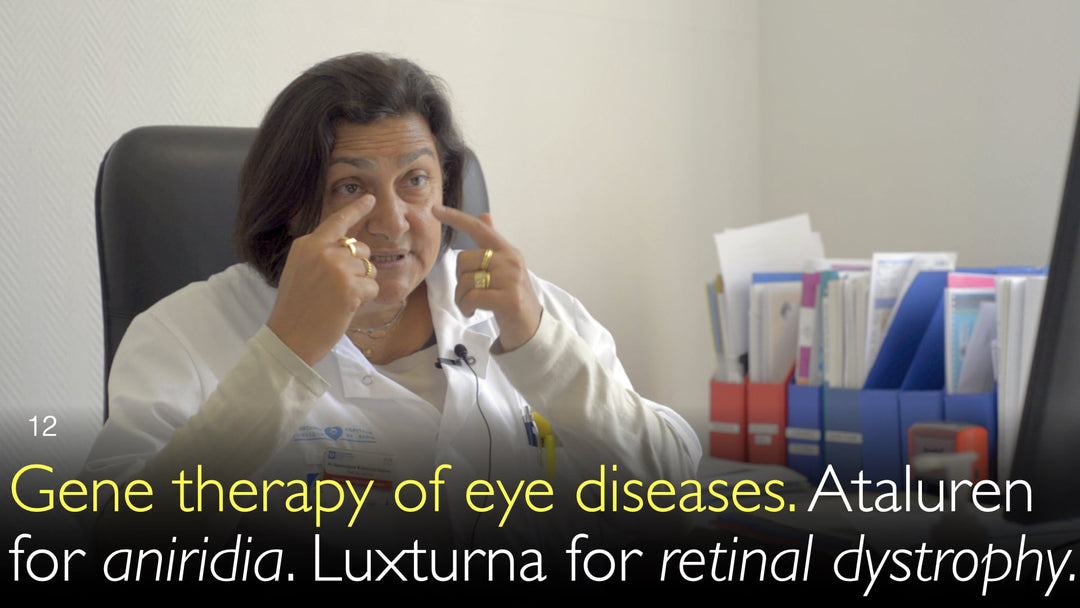
Лукстурна (воретиген непарвовек) — это инновационная генная терапия, одобренная для лечения дистрофии сетчатки, вызванной мутациями в гене RPE65. Доктор медицинских наук Доминик Бремон-Жиньяк объясняет новаторскую концепцию лечения: вирусный вектор доставляет функциональную копию гена RPE65 прямо в клетки сетчатки. Хирургическая процедура предполагает введение вирусного вектора под сетчатку, что позволяет воспроизводить критически важный белок RPE65, которого не хватает у поражённых детей, воздействуя таким образом на саму генетическую причину потери зрения.
Результаты клинических испытаний и исходы лечения пациентов
Первые клинические испытания Лукстурны показали многообещающие результаты. Доктор медицинских наук Доминик Бремон-Жиньяк сообщает об испытании с участием пяти детей с дистрофией сетчатки, получивших это инновационное лечение. Исходы оказались весьма обнадёживающими: у некоторых пациентов зафиксировано значительное улучшение зрения. Эти ранние успехи демонстрируют потенциал генной терапии не только останавливать прогрессирование болезни, но и фактически обращать вспять потерю зрения, предлагая новую парадигму лечения наследственных заболеваний сетчатки.
Аталурен и генная терапия аниридии
Помимо заболеваний сетчатки, подходы генной терапии исследуются и для патологий роговицы, таких как аниридия. Доктор медицинских наук Доминик Бремон-Жиньяк обсуждает Аталурен как ещё одну перспективную стратегию, работающую по схожему принципу преодоления генетических дефектов. Это средство позволяет клеточному аппарату «считывать» преждевременные стоп-кодоны в генетическом коде, благодаря чему становится возможным производство функционального белка. Такой механизм открывает возможности для лечения различных генетических нарушений, вызванных нонсенс-мутациями.
Доктор медицинских наук Доминик Бремон-Жиньяк подчёркивает, что этот подход может быть особенно ценным при заболеваниях роговицы, где традиционные методы лечения ограничены. Способность эффективно «перескакивать» стоп-кодоны для воспроизведения необходимых белков представляет собой тонкое генетическое вмешательство, расширяющее возможности терапии для более широкого спектра глазных патологий.
Будущее генной терапии заболеваний глаз
Область офтальмологической генной терапии всё ещё находится на ранней стадии, но развивается стремительно. Доктор медицинских наук Доминик Бремон-Жиньяк отмечает, что исследователи уже разрабатывают генную терапию, нацеленную на другие мутации помимо RPE65, расширяя потенциальные области применения этой технологии. Интервью с доктором медицинских наук Антоном Титовым показывает, что научное сообщество изучает вирусные векторы и механизмы доставки, которые могли бы сделать эти методы лечения применимыми к различным структурам глаза, включая как сетчатку, так и роговицу.
Как объясняет доктор медицинских наук Доминик Бремон-Жиньяк, уникальные свойства глаза делают его превосходной мишенью для генной терапии. Его изолированность и иммунная привилегированность снижают риск системных побочных эффектов, а доступность позволяет проводить прямое введение лечения. Эти факторы способствуют тому, что офтальмология становится ведущей специальностью в продвижении технологий генной терапии.
Новая надежда для пациентов с редкими заболеваниями глаз
Генная терапия даёт беспрецедентную надежду пациентам с редкими генетическими заболеваниями глаз, которые раньше считались неизлечимыми. Доктор медицинских наук Доминик Бремон-Жиньяк подчёркивает преобразующее воздействие этих методов лечения, особенно на детей, которым грозила полная потеря зрения, а теперь у них есть шанс восстановить функциональное зрение. Это означает фундаментальный сдвиг — от купирования симптомов к воздействию на саму генетическую причину заболевания.
Обсуждение с доктором медицинских наук Антоном Титовым подчёркивает, что генная терапия олицетворяет передовой край медицинской науки, требующий тщательной научной проверки перед клиническим применением. Как заключает доктор медицинских наук Доминик Бремон-Жиньяк, эти достижения вселяют ключевую надежду в бесчисленных пациентов и семьи, затронутые генетическими заболеваниями глаз, знаменуя начало новой эры в офтальмологическом лечении.
Полная расшифровка
Доктор медицинских наук Антон Титов: Генная терапия заболеваний глаз. Каково будущее генной терапии заболеваний глаз? И где сегодня в офтальмологии наблюдается наибольший прогресс в генной терапии?
Доктор медицинских наук Доминик Бремон-Жиньяк: Генная терапия сегодня — это вызов. У нас так много редких заболеваний глаз. Но особенность глазных болезней в том, что глаз — это маленькая лаборатория для медицинских исследований.
Первое фармацевтическое лекарственное средство вот-вот будет одобрено. Оно уже одобрено. Его утвердили в августе для генной терапии заболеваний глаз, в частности сетчатки. Это Лукстурна для мутации RPE65 у детей с дистрофией сетчатки.
Концепция очень интересна, потому что мы используем вирусный вектор и белок, который может реплицироваться внутри сетчатки. Мы вводим под глаз, а точнее под сетчатку, вирусный вектор-носитель, чтобы добиться этой репликации белка RPE65.
Мы только начали это клиническое испытание на детях. У нас пять детей с дистрофией сетчатки, которых лечили Лукстурной. Мы очень довольны, потому что у некоторых из них были очень хорошие результаты.
Я думаю, мы только начинаем прогрессировать. Существуют и другие виды генной терапии, нацеленные на другие мутации.
Также очень интересно знать, что это для сетчатки, но может быть и для роговицы, как мы обсуждали Аталурен для роговицы при аниридии. Это может быть такая генная терапия, просто перепрыгивающая стоп-кодон для репликации белка.
Я думаю, мы только в начальной области генной терапии. Но удивительно, что мы можем представить себе выздоровление пациентов. Дети, которые должны были полностью потерять зрение, теперь могут его восстановить.
Это надежда для пациентов. Для всех нас это очень, очень важно, потому что существует так много болезней, которые нельзя вылечить более традиционными фармацевтическими или хирургическими методами.
Генная терапия представляет собой передовой край науки, и, конечно, она должна применяться на полной научной основе. Несомненно!